壏搙傪偲傕側偭偰婲偙傞懱愊曄壔
|
 塼懱偺懱愊曄壔 塼懱偺懱愊曄壔
丂晛捠偺塼懱偱偼丄壏搙偑忋徃偡傞偲偲傕偵懱愊偼傎傏堦掕偺妱崌偱憹壛偡傞丅
丂悈偺懱愊曄壔
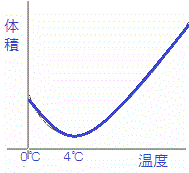
丂悈偼偪傚偭偲摿庩側塼懱偱丄侽亷偐傜係亷傑偱偼壏搙偺忋徃偲偲傕偵懱愊偑尭彮偡傞丅偦偟偰係亷偐傜壏搙偑崅偔側傞偵偮傟偰懱愊偼憹壛偟偰偄偔丅偙偺條巕傪娙扨側僌儔僼偵帵偡偲塃偺傛偆偵側傝丄摨偠廳偝偺悈偱斾傋偨偲偒丄係亷偺悈偑嵟傕懱愊偑彫偝偄偙偲偵側傞丅偙偺懱愊偑嵟彮偺悈侾侽侽侽們倣俁偺廳偝傪侾倠倗偲偡傞偺偑丄崱偺僉儘僌儔儉偺掕媊偺傕偲偵側偭偨傕偺偱偁傞丅
丂悈偐傜昘偵側傞偲偒傕懱愊偺曄壔偑尒傜傟傞丅昘偵側傞偲丄懱愊偼偍傛偦侾.侾攞偵側傞丅偙傟偵傛傝丄朿挘偟偰寉偔側偭偨昘偼悈偵晜偔丅
丂悈偐傜悈忲婥偵側傞偲偒偼丄懱愊偼旕忢偵戝偒偔側傞丅偙偺朿挘乮傏偆偪傚偆丒懱愊偑戝偒偔側傞偙偲乯偺椡傪棙梡偟偨偺偑忲婥婡娭偱偁傞丅
|
|
|
擬偟偵偔偔丂椻傔偵偔偄
|
丂恖娫偺懱撪偵棳傟傞悈偺栶妱偼丄暔幙傪梟偐偟偰塣斃偡傞偩偗偱偼側偄丅懱壏傪曐偮偲偄偆栶妱傕偁傞丅
丂偙傟偼丄悈偺乽擬偟偵偔偔丂偝傔偵偔偄乿偲偄偆摿惈偐傜偱丄悈偺乽斾擬梕検偑崅偄乿偙偲偵傛傞傕偺丅斾擬梕検偲偼丄暔幙偺壏搙傪忋徃偝偣傞偺偵昁梫側僄僱儖僊乕偺偙偲偱丄扨埵偼乽僇儘儕乕傑偨偼僕儏乕儖乿偱昞偡丅悈偺応崌丄廳検侾僌儔儉傪侾亷忋徃偝偣傞偺偵栺侾僇儘儕乕傪梫偡傞丅偲偙傠偑傎偐偺梟塼偼偙偺敿暘偱偡傓丅
丂斾擬梕検偺掅偄暔帒偼丄揝偺傛偆偵乽擬偟傗偡偔丂椻傔傗偡偄乿傕偺偩偐傜丄傕偟悈偑斾擬梕検偺掅偄暔幙偩偭偨傜恖娫偺懱壏偼婥壏偵傛偭偰娙扨偵嵍塃偝傟棎崅壓偡傞偩傠偆丅偡側傢偪丄斾擬梕検偑崅偄偙偲偼乽僄僱儖僊乕傪挋傔偰抲偒傗偡偄乿偙偲傪堄枴偡傞丅
亂1僇儘儕乕佮4.186僕儏乕儖亃
|
|
 丂抧媴偵偼栺侾係壄倠倣3偺悈偑偁傞偲尵傢傟偰傞丅偙偺撪丄栺俋俈亾偑奀悈偱丄扺悈偼俁亾偩偗丅偙偺扺悈偺戝晹暘偼杒嬌傗撿嬌偵偁傞昘偲側偭偰偄傞偐傜丄巹偨偪偑棙梡偡傞偙偲偑偱偒傞愳丒屛偺悈傗抧壓悈偼抧媴忋偺悈偺傢偢偐侽.俁亾偵夁偓側偄丅
丂抧媴偵偼栺侾係壄倠倣3偺悈偑偁傞偲尵傢傟偰傞丅偙偺撪丄栺俋俈亾偑奀悈偱丄扺悈偼俁亾偩偗丅偙偺扺悈偺戝晹暘偼杒嬌傗撿嬌偵偁傞昘偲側偭偰偄傞偐傜丄巹偨偪偑棙梡偡傞偙偲偑偱偒傞愳丒屛偺悈傗抧壓悈偼抧媴忋偺悈偺傢偢偐侽.俁亾偵夁偓側偄丅 丂悈偼惗暔偺庡梫惉暘偱偁傝丄惗暔偺廳偝偺60乣80%偼悈偺廳偝偱偁傞丅
丂悈偼惗暔偺庡梫惉暘偱偁傝丄惗暔偺廳偝偺60乣80%偼悈偺廳偝偱偁傞丅
 塼懱偺懱愊曄壔
塼懱偺懱愊曄壔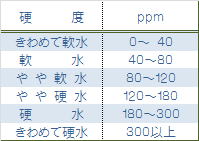 偺斀墳偱捑揳偡傞偨傔丄彍偔偙偲偑偱傞丅
偺斀墳偱捑揳偡傞偨傔丄彍偔偙偲偑偱傞丅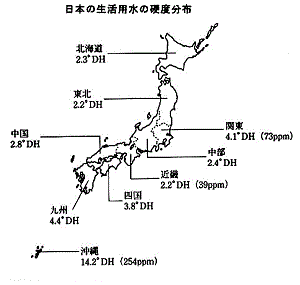
 丂儈僱儔儖偲偼懱偺婡擻偺堐帩丒挷愡偵昁梫晄壜寚側塰梴慺偱偁傞丅恖偺懱偺95%偼桳婡暔乮巁慺丄扽慺丄悈慺丄拏慺乯偱峔惉偝傟偰偍傝丄巆傝偺5%偑柍婡暔丒峼暔偱偁傞儈僱儔儖偱偁傞丅
丂儈僱儔儖偲偼懱偺婡擻偺堐帩丒挷愡偵昁梫晄壜寚側塰梴慺偱偁傞丅恖偺懱偺95%偼桳婡暔乮巁慺丄扽慺丄悈慺丄拏慺乯偱峔惉偝傟偰偍傝丄巆傝偺5%偑柍婡暔丒峼暔偱偁傞儈僱儔儖偱偁傞丅
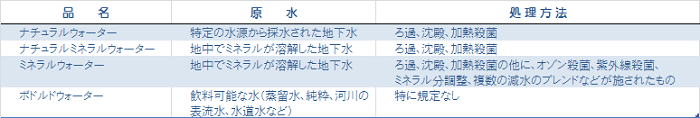
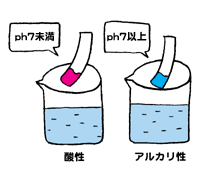 丂傛偔帹偵偡傞乽巁惈乿偲乽傾儖僇儕惈乿丅偙傟傪昞偡扨埵傪乽pH乮儁乕僴乕乯乿偲尵偆丅
丂傛偔帹偵偡傞乽巁惈乿偲乽傾儖僇儕惈乿丅偙傟傪昞偡扨埵傪乽pH乮儁乕僴乕乯乿偲尵偆丅